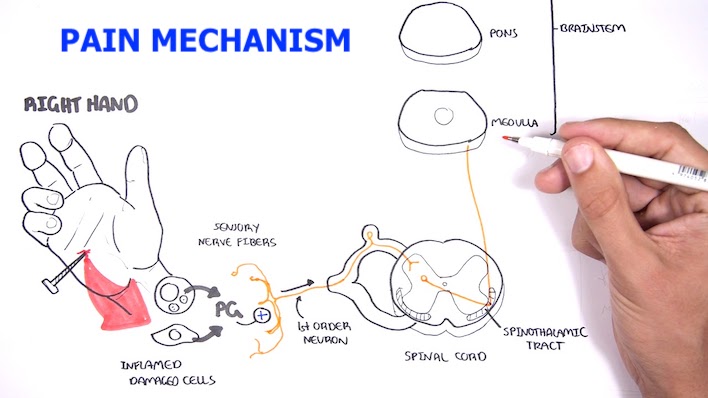
Bước đầu tiên để hiểu sinh lý học của đau là phân biệt đau (pain) với cảm thụ đau (nociception). Cảm thụ đau được định nghĩa là “quá trình thần kinh mã hóa các kích thích độc hại.” Cường độ của các tín hiệu cảm thụ đau được cho là tỷ lệ thuận với các kích thích ban đầu của chúng. Tuy nhiên, việc truyền các tín hiệu cảm thụ đau có thể được tạo thuận hoặc bị ức chế tại một số vị trí trong hệ thống cảm thụ đau trước khi nhận biết có ý thức để cuối cùng chúng có thể được cảm nhận là đau hay không.
Cơ quan thụ cảm đau (Nociceptor)
Nociceptor là các đầu tận cùng dây thần kinh tự do có trong hầu hết các loại mô. Tương tự như các đầu tận cùng của dây thần kinh khác, chúng được kích hoạt bởi các kích thích cơ học, nhiệt và hóa học, nhưng các cơ quan thụ cảm đau có thể mã hóa các kích thích đó thành độc hại. Cơ quan thụ cảm đau tạo ra điện thế hoạt động khi các kênh ion trong màng tế bào được kích hoạt bởi một kích thích đủ lớn.
Độ nhạy của một nociceptor có thể thay đổi. Khi các nociceptor được kích hoạt, chúng giải phóng các chất như neuropeptide, glutamate và cytokine vào các mô xung quanh. Những chất này có thể hạ thấp ngưỡng kích hoạt của tất cả các nociceptor trong vùng đó và mở rộng vùng tiếp nhận của chúng. Sự tạo thuận cho cảm thụ đau ở mức này được gọi là sự nhạy cảm hoá/mẫn cảm ngoại biên (peripheral sensitization). Sự nhạy cảm hoá ở ngoại biên cho phép những kích thích không độc hại kích hoạt đầu vào cảm thụ đau. Đây có thể là một khía cạnh thích ứng bình thường của phản ứng của mô với chấn thương, thường sẽ tự hết trong vài ngày hoặc vài tuần, nhưng nếu tình trạng nhạy cảm hoá ngoại vi không tự khỏi thì có thể được xem là một tình trạng thích ứng kém.
Các tế bào thần kinh hướng tâm sơ cấp (Primary Afferent Neurons)
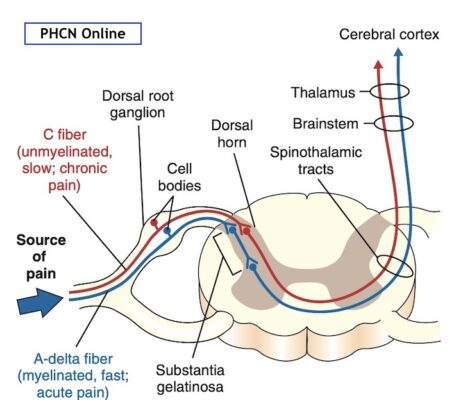
Các tín hiệu cảm thụ đau được truyền đến thần kinh trung ương bởi các tế bào thần kinh hướng tâm sơ cấp. Mỗi tế bào thần kinh này bao gồm một thân tế bào ở một trong các hạch rễ lưng, một nhánh ngoại biên là sợi trục dẫn đến đầu tận dây thần kinh trong mô đích và một nhánh trung tâm dẫn đến tủy sống. Có ba loại tế bào thần kinh hướng tâm sơ cấp: sợi C, sợi A-delta và sợi A-beta, nhưng chỉ có sợi C và sợi A-delta thường có chức năng cảm thụ đau.
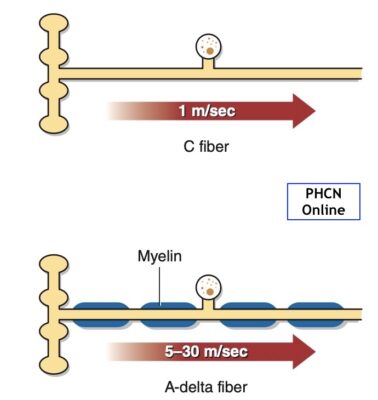
- Các sợi C, còn được gọi là sợi hướng tâm nhóm IV, là những sợi thần kinh nhỏ không có bao myelin truyền điện thế hoạt động tương đối chậm – ở tốc độ 1,0 đến 4,0 m / giây. Sợi C truyền những cảm giác thường được mô tả là âm ỉ, đau nhịp đập, nhức nhối hoặc bỏng rát và có thể được mô tả là tê rần (Hình 1). Đau được dẫn truyền chủ yếu do sợi C có khởi phát chậm sau kích thích độc hại ban đầu, kéo dài, có xu hướng khu trú lan tỏa đặc biệt khi kích thích mạnh, và thường gây khó chịu cho bệnh nhân về mặt cảm xúc. Những cảm giác này thường đi kèm với các phản ứng tự chủ như đổ mồ hôi, tăng nhịp tim và huyết áp, hoặc buồn nôn. và sự giảm đau này bị chặn bởi chất kháng thụ thể opioid như naloxon.
- Các sợi A-delta, còn được gọi là sợi hướng tâm nhóm III, là những sợi có myelin đường kính nhỏ truyền điện thế hoạt động nhanh hơn sợi C — ở khoảng 30 m / giây. Sợi A-delta nhạy cảm nhất với kích thích cơ học cường độ cao nhưng cũng có thể đáp ứng với kích thích nhiệt nóng hoặc lạnh. Cảm giác đau liên quan đến hoạt động của sợi A-delta thường được mô tả là sắc nhọn, như bị đâm hoặc châm chích. Những cảm giác đau này khởi phát nhanh chóng sau kích thích độc hại, chỉ kéo dài trong một thời gian ngắn, thường khu trú ở vùng bị kích thích, và thường không liên quan đến cảm xúc. Đau liên quan đến hoạt hóa sợi A-delta nói chung không bị chặn bởi opioid.
- Các sợi A-beta thường truyền các cảm giác không đau như rung, kéo căng da và cảm thụ cơ học. Sợi A-beta có các đầu tận dây thần kinh chuyên biệt của chúng nằm trong da, xương và khớp và các sợi trục có myelin tương đối lớn cho phép chúng dẫn truyền xung động nhanh hơn so với sợi A-delta hoặc C. Bởi vì sợi A-beta truyền đầu vào không phải cảm thụ đau, sợi A-beta thường không gây ra cảm giác đau trừ khi đầu vào được thu nhận vào hệ thống cảm thụ đau bởi thần kinh trung ương nhạy cảm hoá cao.
Nói chung, khoảng 50% sợi cảm giác trong dây thần kinh ở da có chức năng cảm thụ đau, 19 – 80% trong số này là các sợi C, và 20% còn lại là sợi A-delta. Điện thế hoạt động gây ra bởi chấn thương cơ học thường đi qua các sợi C và A -delta. Lấy ví dụ về một viên gạch rơi vào chân một ai đó. Gần như ngay lập tức, người đó cảm thấy một cảm giác đau nhói. Sau đó là một đau nhức sâu có thể kéo dài vài giờ hoặc vài ngày. Cảm giác sắc nhọn ban đầu được truyền bởi các sợi A-delta phản ứng với kích thích cơ học cường độ cao của các cơ quan thụ cảm do tác động của viên gạch. Cảm giác đau nhức sâu sau đó được truyền qua các sợi C và bị kích thích bởi các chất trung gian hóa học của quá trình viêm được giải phóng sau chấn thương ban đầu, cũng như do kích thích cơ học.
Tính chất đau không chỉ phụ thuộc vào loại sợi dây thần kinh ngoại biên được kích hoạt mà còn loại mô xuất phát kích thích. Đau từ kích thích độc hại ở da thường được cảm nhận là sắc nhọn, tê rần và dễ định vị. Đau từ các cấu trúc cơ xương khớp thường âm ỉ, nặng, hoặc nhức nhối và khó định vị hơn. Đau từ các tạng thì tương tự như đau cơ xương nhưng có xu hướng nông hơn.
Khi các dây thần kinh ngoại biên bị tổn thương, chúng có thể tạo ra và truyền các xung động. Khi các màng tế bào thần kinh bị gián đoạn, các kênh ion trôi nổi tự do trong chất dịch nội thần kinh đôi khi tự chèn vào khu vực bị gián đoạn. Các vị trí này, được gọi là các vị trí tạo xung động bất thường (abnormal impulse-generating sites, AIGS), khi đó có thể tạo ra các xung động cảm giác đau để đáp lại các kích thích tương đối nhỏ.
Khi vỏ các bó thần kinh (epineurium) bị tổn thương do tác động cơ học hoặc hóa học, nó có thể bị viêm giống như bất kỳ mô nào khác và dây thần kinh cảm giác bao quanh (nervi nervorum) có thể trở nên nhạy cảm. Phù nội thần kinh khi đó làm tăng áp lực nội thần kinh, làm giảm sự lưu thông của dịch nội thần kinh và máu bên trong dây thần kinh. Sự phóng điện cảm thụ đau bất thường từ AIGS, tăng độ nhạy của nervi nervorum trong nội thần kinh và giảm lưu thông tuần hoàn nội thần kinh được cho là những cơ chế chính gây ra đau thần kinh ngoại biên.
Các đường truyền trung ương (Central Pathways)
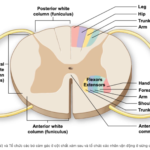
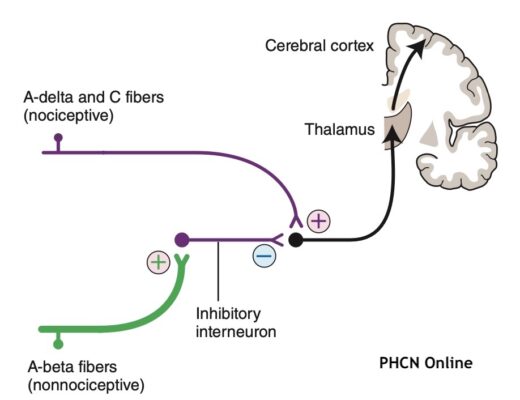
Các tế bào thần kinh hướng tâm sơ cấp chiếu tới sừng lưng của chất xám của tủy sống (substantia gelatinosa) (Hình 2). Sừng lưng được tổ chức thành sáu lớp (laminae) chia tách các tín hiệu theo nguồn đến của chúng. Lớp 1, 2 và 5 nhận đầu vào từ sợi C và A-delta, trong khi sợi A-beta kết thúc ở lớp 3 và 4. Sừng lưng là vị trí đầu tiên trong thần kinh trung ương nơi các tín hiệu cảm thụ đau được tích hợp với đầu vào từ các sợi hướng tâm sơ cấp khác, các neuron trung gian (interneurons) tại chỗ từ bên trong tủy sống, và tín hiệu đi xuống từ não. Quá trình này có thể dẫn đến việc tạo thuận hoặc ức chế việc truyền đầu vào cảm thụ đau và không cảm thụ, cũng như trong một số trường hợp, thay đổi đầu vào không cảm thụ thành đầu vào cảm thụ đau. Khi quá trình truyền được tạo thuận, nó có khả năng gây ra cảm giác đau dữ dội hơn. Việc ức chế các tín hiệu cảm thụ có tác dụng ngược lại, làm giảm hoặc ngăn chặn hoàn toàn cảm giác đau. Một cơ chế của điều này là ức chế trước synap của các interneurons trong tủy sống bằng đầu vào không cảm thụ (Hình 3). Đây là bản chất của lý thuyết kiểm soát cổng để điều biến đau. Nhiều tác nhân vật lý cũng như các biện pháp can thiệp khác được cho là kiểm soát cơn đau một phần bằng cách cung cấp đầu vào không cảm thụ cho các dây thần kinh cảm giác, do đó ức chế sự hoạt hóa của các tế bào thần kinh cảm thụ và “đóng cổng” dẫn truyền cảm thụ đau ở tủy sống.
Hệ thống opioid nội sinh
Nhận cảm đau cũng được điều chỉnh bởi các peptide giống như opioid nội sinh. Các peptide này được gọi là opiopeptins (trước đây được gọi là endorphin) và kiểm soát đau bằng cách liên kết với các thụ thể opioid đặc hiệu trong hệ thần kinh. Hệ thống giảm đau nội sinh này lần đầu tiên được phát hiện vào năm 1973 khi ba nhóm nhà nghiên cứu độc lập đang điều tra cơ chế giảm đau do morphin đã phát hiện ra các vị trí gắn opioid cụ thể trong thần kinh trung ương. Sau đó, người ta tìm thấy hai peptit — met-enkephalin (methionine-enkephalin) và leu-enkephalin (leucine-enkephalin) —được phân lập từ thần kinh trung ương của lợn cũng gắn với các vị trí gắn opioid này. Các enkephalin này tạo ra các tác dụng sinh lý tương tự như của morphin, và tác dụng và sự gắn của chúng là bị chặn bởi chất đối kháng opioid naloxone. Kể từ đó, các nhà nghiên cứu đã xác định và phân lập các opiopeptins khác, bao gồm beta-endorphin và dynorphin A và B. Các opiopeptins và các thụ thể opioid có trong nhiều đầu dây thần kinh ngoại vi và trong tế bào thần kinh ở một số vùng của hệ thần kinh. Opiopeptins và các thụ thể opioid được tìm thấy trong chất xám quanh cống não (PAGM) và nhân raphe của thân não — các cấu trúc gây giảm đau khi được kích thích bằng điện. Nồng độ cao của opiopeptins cũng được tìm thấy trong các lớp ngoài của sừng lưng của tủy sống (lớp I và II), trong các khu vực khác nhau của hệ limbic, và trong hệ thần kinh ruột, cũng như trong các đầu tận dây thần kinh sợi C.
Opioid và opiopeptins có tác dụng ức chế. Chúng gây ức chế trước synap bằng cách ức chế dòng ion canxi đi vào và gây ức chế sau synap bằng cách thúc đẩy dòng ion kali ra ngoài. Ngoài ra, opiopeptins còn gián tiếp ức chế sự truyền dẫn cảm giác bằng cách ức chế sự giải phóng axit gamma-aminobutyric (GABA) trong PAGM và nhân raphe. GABA ức chế hoạt động của các cấu trúc kiểm soát cơn đau khác nhau bao gồm các liên kết A-beta, PAGM và nhân raphe và do đó có thể làm tăng truyền dẫn cảm thụ đau trong tủy sống.
Kích thích điện các khu vực có hàm lượng opiopeptins cao, chẳng hạn như PAGM và nhân raphe, ức chế mạnh mẽ sự truyền thụ cảm của các tế bào thần kinh sừng ở lưng tủy sống, do đó làm giảm đau. kích thích điện những vùng não này có thể làm giảm đau khó trị và có thể làm tăng lượng beta-endorphin trong dịch não tủy (CSF). Nồng độ của các thụ thể opioid và opiopeptins trong hệ thống limbic , một khu vực của não phần lớn liên quan đến các hiện tượng cảm xúc, cũng giải thích cho phản ứng cảm xúc đối với cơn đau và sự hưng phấn và giảm căng thẳng cảm xúc liên quan đến việc sử dụng morphin và giải phóng opiopeptins.
Việc giải phóng opiopeptins được cho là đóng một vai trò quan trọng trong việc điều chỉnh và kiểm soát cơn trong thời gian căng thẳng về cảm xúc.
Lý thuyết opioid nội sinh cũng đem lại một lời giải thích khả thi cho tác dụng giảm đau nghịch lý của kích thích đau và châm cứu. Mức độ kích thích đau đớn có thể chịu đựng được chẳng hạn như các chế phẩm tại chỗ gây ra cảm giác bỏng rát hoặc kích thích dây thần kinh bằng điện qua da (TENS) gây ra cảm giác châm chích hoặc bỏng rát đã được chứng minh là làm giảm cường độ đau ở vùng bôi thuốc và trong các khu vực khác. Tác dụng giảm đau với giả dược cũng được cho là một phần do opiopeptins trung gian, vì chất đối kháng opioid naloxone có thể đảo ngược tác dụng giảm đau với giả dược và giả dược cũng có thể gây ức chế hô hấp, một tác dụng phụ điển hình của opioid
Nhạy cảm hóa trung ương (Central Sensitization)
Nhạy cảm hóa trung ương đề cập đến sự tạo thuận các xung cảm thụ đau ở hệ thần kinh trung ương. Có ba khía cạnh đối với sự nhạy cảm hóa trung ương: (1) tạo thuận cho dẫn truyền qua synap trong tủy sống, (2) ức chế hệ thống opioid nội sinh và (3) thay đổi quá trình xử lý cảm giác đau trong não. Nhạy cảm hoá trung ương có thể gây đau và các cảm giác khó chịu khác thường không chỉ giới hạn trong phân bố thần kinh ngoại vi hoặc giải phẫu và có phản ứng không nhất quán với hoạt động thể chất hoặc căng thẳng. Nhạy cảm trung ương thường được bắt đầu bởi một kích thích cảm thụ đau nhưng, một khi đã được thiết lập, có thể tiếp tục vô thời hạn mà không hoặc chỉ có rất ít kích thích ngoại vi.
Những thay đổi tế bào và phân tử liên quan đến nhạy cảm hóa trung tâm lý bao gồm sự thay đổi chức năng trong tính kích thích ở synap giữa các tế bào thần kinh hướng tâm sơ cấp và thứ cấp, sự thích nghi trong tế bào microglia (tế bào thần kinh đệm nhỏ), tế bào hình sao, tăng tính kích thích màng tế bào thần kinh và những thay đổi trong quá trình dịch mã gen. Trong một số trường hợp, sợi C chết lùi từ lớp 2 ở sừng lưng và được thay thế bằng sợi A-beta, chuyển hướng đầu vào hướng tâm cảm giác không cảm thụ sang các cảm thụ đau. Điều này làm cho các đầu vào từ các cảm giác không đau như nóng , lạnh hoặc căng được chuyển đổi thành tín hiệu cảm thụ, có khả năng gây ra trải nghiệm đau.
Đặc điểm quan trọng nhất của nhạy cảm trung tâm là nó dẫn đến các triệu chứng của bệnh nhân không còn phản ánh một cách đáng tin cậy trạng thái của các mô.
Điều biến cảm thụ đau ở não (Modulation)
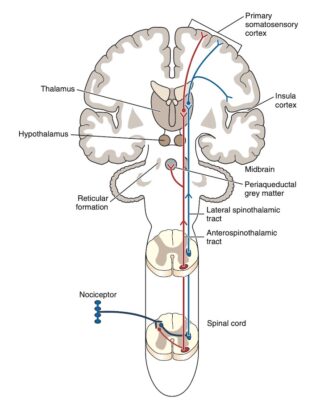
Tín hiệu vào cảm thụ đau được truyền từ sừng lưng của tủy sống đến não qua một số đường truyền lên, chủ yếu là bó gai đồi thị (Hình 4) . Khi đã ở đến não, đầu vào được phân phối đến nhiều cấu trúc cảm giác, vận động và hệ viền bao gồm vỏ não cảm giác thân thể sơ cấp và thứ cấp. vỏ não tiền vận động vỏ vận động, và vỏ não trước, thuỳ gai phần trước (anterior cingulate) và thuỳ đảo, đồi thị, và vỏ não trước trán. Nhóm này đôi khi được gọi là ma trận đau (pain matrix).
Ma trận đau được cho là tạo ra ba đầu ra riêng biệt để đáp ứng với cảm thụ đau. Đầu ra đầu tiên là nhận biết có ý thức hoặc trải nghiệm về một cơn đau. Đây là thời điểm mà cảm thụ đau được chuyển thành đau. Đầu ra thứ hai là hoạt động thể chất, bao gồm các phản ứng vận động như căng cơ hoặc vận động hoặc phản ứng hành vi. Đầu ra thứ ba là kích hoạt hệ thống tự chủ, nội tiết và miễn dịch, được gọi chung là hệ thống cân bằng nội môi. Mỗi đầu ra từ ma trận đau được cho là được lập chương trình trước theo di truyền ở trong não nhưng liên tục được điều chỉnh theo các hoàn cảnh. Thuyết này giải thích các trường hợp đau chi ma là những trường hợp mà đầu vào cảm thụ đau không thể đến não.
Cũng như trong tủy sống, sự điều biến của cảm thụ đau trong ma trận đau là một quá trình động. Các yếu tố nhận thức, cảm xúc, xã hội và ngữ cảnh thay đổi đầu vào. Quá trình giải thích cảm thụ đau và tạo ra trải nghiệm đau kích thích não bộ phát triển về mặt chức năng và hình thái theo thời gian. Ví dụ, đau mạn tính kích hoạt vỏ não trước trán nhiều hơn so với đau cấp tính, ngụ ý ảnh hưởng mạnh mẽ hơn đến nhận thức, cảm xúc và hướng nội.
Một trong những yếu tố quan trọng nhất ảnh hưởng đến quá trình xử lý cảm thụ đau của ma trận đau là việc đánh giá vô thức mức độ đe dọa của kích thích ban đầu đối với cơ thể. Khi mối đe dọa mức độ liên quan đến kích thích được cho là thấp, bất kỳ đầu vào kích thích nào có nhiều khả năng bị lọc ra, bởi hệ thống opioid đi xuống hoặc đồi thị. Nếu mức độ đe dọa được cho là cao, ma trận đau có nhiều khả năng phản ứng với trải nghiệm đau, hành vi và một phản ứng của hệ thống cân bằng nội môi. Do đó, một người có thể không nhận thấy một chấn thương nhỏ trong một tình huống gây căng thẳng khác, chẳng hạn như khi chạy khỏi một toà nhà đang cháy hoặc chơi thể thao, hoặc một người quá cẩn trọng có thể biểu hiện quá nhạy cảm với các kích thích không độc hại, đặc biệt nếu tình huống liên quan đến chấn thương trước đó. Điều quan trọng trong quản lý cơn đau là tránh phóng đại mức độ đe dọa mà bệnh nhân nhận thấy có liên quan đến tình trạng đau của họ.
Lược dịch từ: Physical Agents in Rehabilitation, Michelle H. Cameron, Elsevier, 2018.
KIỂM TRA KIẾN THỨC: SINH LÝ ĐAU
TÓM LƯỢC ĐIỂM QUAN TRỌNG (KEY POINTS)
Để hiểu về sinh lý đau, chúng ta cần phân biệt rõ 3 khái niệm và quy trình sau:
- Cảm thụ đau (Nociception) ≠ Đau (Pain): Cảm thụ đau là quá trình thần kinh mã hóa kích thích độc hại (cơ học, nhiệt, hóa học). Đau là trải nghiệm cảm giác và cảm xúc mang tính chủ quan. Không phải mọi tín hiệu cảm thụ đau đều dẫn đến cảm giác đau (do cơ chế ức chế).
- Hai loại sợi dẫn truyền chính:
- Sợi A-delta: Có bao myelin, dẫn truyền nhanh. Gây ra cảm giác đau “cấp”, nhói, khu trú rõ.
- Sợi C: Không có bao myelin, dẫn truyền chậm. Gây ra cảm giác đau “mạn”, âm ỉ, rát bỏng, khu trú kém.
- Thuyết Kiểm soát Cổng (Gate Control Theory): Tại sừng sau tủy sống, các sợi thần kinh hướng tâm không gây đau (sợi A-beta – như xoa bóp, nhiệt) có thể ức chế việc truyền tín hiệu đau từ sợi A-delta và sợi C. Đây là cơ sở lý thuyết cho nhiều phương pháp vật lý trị liệu.
- Hệ thống ức chế xuống (Descending Inhibition): Não bộ không chỉ nhận tín hiệu mà còn có khả năng giải phóng các opioid nội sinh (endorphin, enkephalin) để “khóa” tín hiệu đau ngay từ mức độ tủy sống.